- Хроматографические стеклянные колонки
- Виды стеклянных хроматографических колонок
- Как купить стеклянные хроматографические колонки
- Колонки лабораторные стеклянные
- Колонка АДС для определения витамина В1 эскиз 2-439
- Колонка адсорбционная (эскиз 5-299)
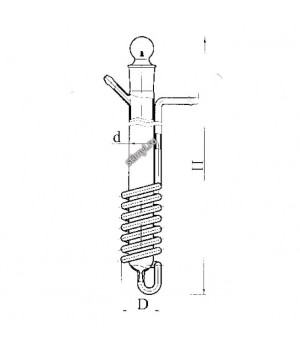
- Колонка для окисления нефтяных масел
- Колонка для определения массовой доли кофеина
- Колонка для парафинов ГФ 6.150.152
- Колонка для хроматографического разделения нефтепродуктов эскиз 2-160
- Колонка ионообменная, эскиз 2-707
- Колонка к хроматографу, эскиз 2-617
- Колонка с краном и фильтром, эскиз 2-909
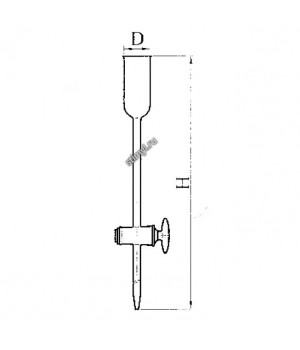
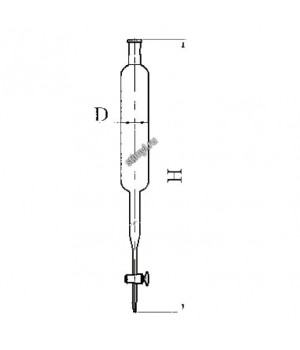
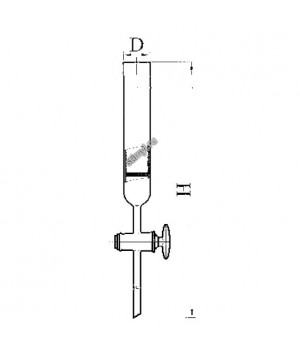
- Колонка с краном эскиз 2-629
- Колонка с краном эскиз 2-654
- Колонка с тефлоновым краном, эскиз 2-900
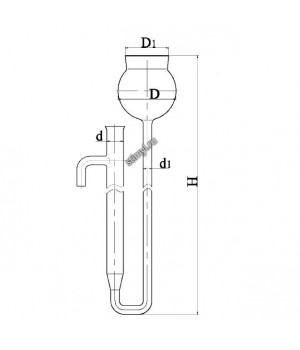
- Колонка с фильтром, эскиз 5-190
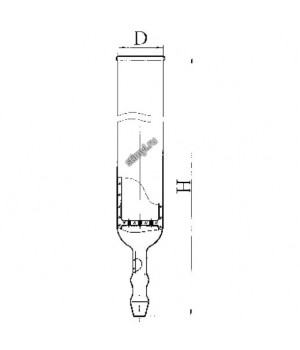
- Колонка сорбционная
- Колонка сорбционная эскиз 2-446
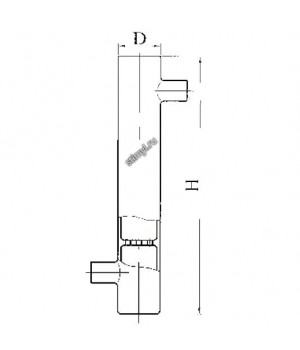
- Колонка сорбционная эскиз 2-883
- Колонка хроматографическая (эскиз 1-78)
- Колонка хроматографическая c ФКП-20-ПОР 40 (эскиз 2-912-01)
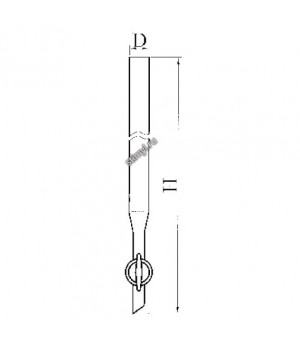
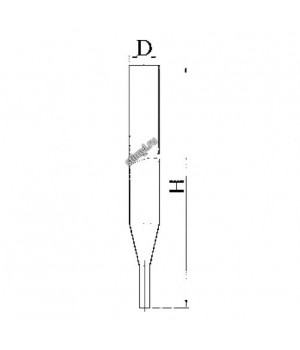
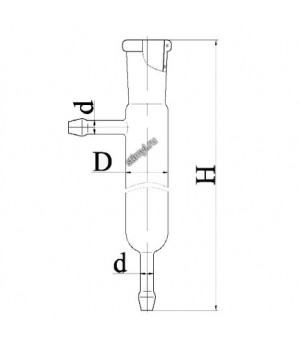
- Стеклянная колонка с оттянутым концом
- Как делить всякое: все, что вы хотели, но боялись спросить о хроматографии. Часть 2. Колоночная хроматография
- Лига Химиков
- Правила сообщества
- Оксид серы. Способы получения и химические свойства
- Выпаривание растворителя из вязкой фосфорорганической кислоты
- Кристаллы уксусной кислоты
- Кристаллы продукта реакции фенольного соединения и свободного радикала
- Добро пожаловать в органическую химию!
- Кристаллы 4-бензоилокси-2,2,6,6-тетраметилпиперидин-1-оксила
- Кристаллы 1-этинил-1-циклогексанола
- Тонкослойная хроматография чернил в ускоренной съемке
- Тонкослойная хроматография для не-специалистов
Хроматографические стеклянные колонки
При работе с химикатами нередко требуется разделение и вычленение отдельных химических соединений. Это производится в лабораторных условиях с помощью специального аппарата — колоночного хроматографа. Данный лабораторный прибор позволяет очистить различные объёмы смесей, без угрозы перекрёстного загрязнения. Используя высококачественные хроматографические колонки можно существенно уменьшить размеры и стоимость неподвижной фазы. Купить стеклянные хроматические колонки вы можете на сайте himbio.ru компания «ХимБиоБезопасность», которая занимается реализацией лабораторного оборудования и стеклянной химпосуды на территории России.
Виды стеклянных хроматографических колонок
Стеклянные хроматографические колонки отличаются по размерам. От диаметра зависит объём используемой смеси и количество вещества, получаемого по итогу очистки. Длина хроматографической колонки влияет на длительность проведения химанализа.
Также хроматографические колонки бывают насадочными и капиллярными. Последняя разновидность более распространена благодаря отличным техническим характеристикам и соответствию нормам работы в лабораторных условиях. Некоторые модели лабораторных хроматографических колонок оснащены специальными краниками.
Хроматографические колонки могут изготавливаться из разных материалов, но самым популярные — стеклянные, так как стекло:
- инертно, не вступает в реакции практически ни с какими другими химическими веществами;
- имеет крайне высокую температуру плавления, поэтому в стеклянной посуде можно проводить различные химические манипуляции при высоких температурах;
- прозрачная стеклянная посуда позволяет наблюдать за протеканием химических реакций и контролировать их.
Как купить стеклянные хроматографические колонки
Лабораторные приборы — это особая категория товаров, недоступная для широкого пользователя. Качественное и профессионально лабораторное оборудование и стеклянную посуду вы можете заказать на сайте Центра научно-технического сотрудничества «ХимБиоБезопасность». Наша компания сотрудничает с мировыми производителями лабораторного оборудования, чья продукция проходит многоуровневый контроль качества и отличается высочайшим качеством и надёжностью материалов.
Источник
Колонки лабораторные стеклянные
Код товара: 387-01
Колонка АДС для определения витамина В1 эскиз 2-439
Колонка АДС для определения витамина В1 эскиз 2-439 ШифрD ммН ммТип крана119530300К1Х-1-28-1.6..
Код товара: 327-01
Колонка адсорбционная (эскиз 5-299)
Код товара: 164-01
Колонка для окисления нефтяных масел
Предназначена для определения стабильности масел против окисления в соответствии с требованиями ГОСТ..
Код товара: 165-01
Колонка для определения массовой доли кофеина
Колонка для определения массовой доли кофеина применяется для определения массовой доли кофеина. Шиф..
Код товара: 386-01
Колонка для парафинов ГФ 6.150.152
Колонка для парафинов ГФ 6.150.152 ШифрD ммН ммТип кранаШлиф КШ по ГОСТ 8682-932728501410К1Х-1-28-1.
Код товара: 396-01
Колонка для хроматографического разделения нефтепродуктов эскиз 2-160
Колонка для хроматографического разделения нефтепродуктов эскиз 2-160 ШифрD ммН мм199914300..
Код товара: 388-01
Колонка ионообменная, эскиз 2-707
Колонка ионообменная, эскиз 2-707 ШифрD ммН ммТип крана296328265К1Х-1-28-1.6..
Код товара: 394-01
Колонка к хроматографу, эскиз 2-617
Колонка к хроматографу, эскиз 2-617 ШифрD ммН мм278024500..
Код товара: 328-01
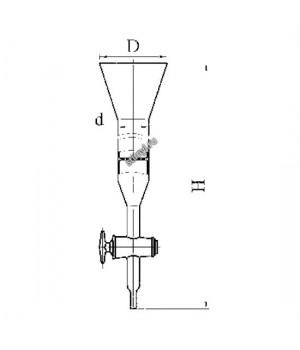
Колонка с краном и фильтром, эскиз 2-909
Код товара: 385-01
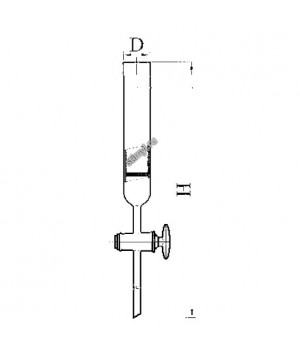
Колонка с краном эскиз 2-629
Колонка с краном эскиз 2-629 ШифрD ммН ммd ммТип крана28043034530К1Х-1-40-4,0..
Код товара: 166-01
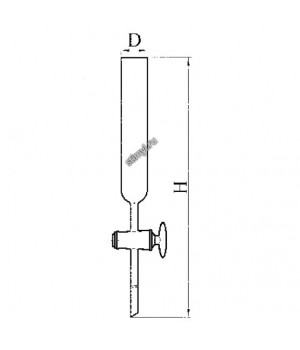
Колонка с краном эскиз 2-654
Колонка с краном изготавливаются из стекла Симакс ЧСН ИСО 3585. ШифрD ммН ммТип крана286024320К1Х-1-..
Код товара: 329-01
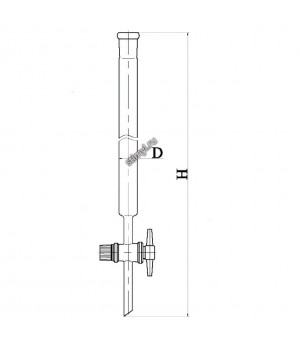
Колонка с тефлоновым краном, эскиз 2-900
Код товара: 384-01
Колонка с фильтром, эскиз 5-190
Колонка с фильтром, эскиз 5-190 ШифрD ммН ммТип кранаПористость фильтра ФКП-40645315К1Х-1-32-2,5ПОР ..
Код товара: 167-01
Колонка сорбционная
Колонка сорбционная — внутри колонок впаяны плоские стеклянные пластины, имеющие 9 отверстий диаметр..
Код товара: 389-01
Колонка сорбционная эскиз 2-446
Колонка сорбционная эскиз 2-446 ШифрD ммН мм103424150..
Код товара: 390-01
Колонка сорбционная эскиз 2-883
Колонка сорбционная эскиз 2-883 Шифр — 3418..
Код товара: 392-01
Колонка хроматографическая (эскиз 1-78)
Колонка хроматографическая (эскиз 1-78) Шифр D мм Н мм Шлиф КШ по ГОСТ 86..
Код товара: 330-01
Колонка хроматографическая c ФКП-20-ПОР 40 (эскиз 2-912-01)
Колонки лабораторные – стеклянные приспособления, предназначенные для разделения смесей химических веществ и проведения работ по определению каких-либо веществ, например, определение витаминов, анализ нефтяных масел, парафинов, нефтепродуктов, кофеина и т.д.
Представляют собой длинную стеклянную трубку с узкой нижней частью, в которой может находиться кран или зажим для регулирования скорости вытекания жидкости, отводок, фильтр и т.д.
Самые распространенные виды хроматографических колонок:
- насадочные;
- капиллярные;
- с кранами или без кранов;
- с фильтрами или без фильтров;
- ионообменные;
- сорбционные и т.д.
Выполняются из специального стекла — инертного к химическим веществам и термостойкого.
Размеры и типы колонок зависят от вида анализа и количества разделяемых веществ и подбираются индивидуально под каждый вид работ в зависимости от решаемых задач и условий проведения исследования.
Источник
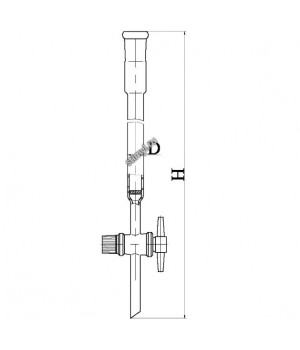
Стеклянная колонка с оттянутым концом
Ионообменные колонки (рис. 115) бывают разнообразных типов. Колонки, используемые в качественном анализе неорганических веществ, представляют собой трубки длиной 100—120 мм, с внутренним диаметром 3—6 мм. Перед использованием колонки нижний конец ее закрывают ватным тампоном.
Рис. 113. Общий вид хроматографа 
Адсорбенты (в большинстве случаев для качественного анализа неорганических веществ используют «окись алюмнния для хроматографии») помещают в колонку при помощи стеклянных воронок диаметром 30—50 мм, с оттянутым нижним концом. Адсорбент вносят в колонку сразу всей порцией, после чего слой его уплотняют на ручной центрифуге (75 об/мин) или вручную постукиванием о твердую поверхность.
Рис. 114. Камеры для получения хроматограмм на бумаге: а — одномерной восходящей: б — нисходящей — на узкой полосе бумаги; в — восходящей — на широкой полосе бумаги; г — нисходящей; д — двумерной при одновременном анализе серии отдельных проб: 1 — стеклянный сосуд или кювета; 2 — крышка (пробка); 3 — зажим для бумаги; 4 — бумага; 5 — фронт растворителя; 6 — начальная линия; 7— подвижный растворитель; 8 — бюкс с неподвижным растворителем; 9 — стеклянные перекладины; 10 — рамка для листов бумаги.
После уплотнения адсорбент должен занимать приблизительно половину объема колонки. Окись алюминия вносят в колонку в сухом виде. Растворы в колонку вносят пипетками с оттянутыми капиллярными концами. Фильтраты собирают в пробирки, применяемые в качественном полумикрометоде. В литературе описаны автоматические коллекторы для сбора фракций фильтратов при хроматографическом анализе.
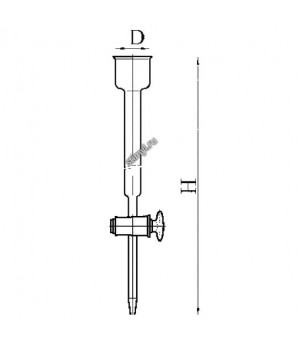
Для ионообменной хроматографии в количественном анализе применяют в большинстве случаев стеклянные колонки высотой 200—300 мм и диаметром 10—20 мм, имеющие в нижней части дренажное устройство (стеклянная пластинка с отверстиями) и кран для регулирования скорости вытекания жидкости.
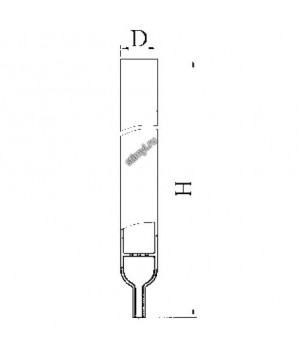
Колонкой может служить стеклянная трубка с оттянутым нижним концом (диаметр 5 мм), на который надевают резиновую трубку. Скорость протекания жидкости через колонку в этом случае регулируется винтовым зажимом на трубке. Колонкой может служить бюретка, применяемая в объемном анализе, емкостью 25, 50 и 
В тех случаях, когда при анализе приходится использовать фтористоводородную кислоту, колонки изготавливают из пластмасс.
Рис. 115. Колонки для ионообменной хроматографии: а — для качественного анализа индивидуальных веществ; б — для хроматографического разделения ионов.
Для регенерации и промывки ионита в колонке ее присоединяют к склянке с нижним тубусом, наполненной регенерирующим раствором. Скорость протекания жидкости через ионит регулируют винтовым зажимом.
Колонки заполняют ионитами во влажном состоянии. Для этого сухой ионит помещают в стакан, заливают дистиллированной водой и оставляют стоять на 30 мин для набухания зерен, затем отмывают декантацией от пыли и постепенно переносят ионит в стеклянную колонку. В колонку помещают предварительно небольшое количество воды, чтобы предотвратить попадание пузырьков воздуха. Если в слой ионита попадают пузырьки воздуха, то образуются каналы, понижающие эффективность действия ионообменной колонки.
Источник
Как делить всякое: все, что вы хотели, но боялись спросить о хроматографии. Часть 2. Колоночная хроматография
Дисклеймер: пост адресуется в основном студентам-химикам, а также может быть интересен для тех, кто когда-либо задавался вопросом, а чем вообще занимаются эти химики в своих лабораториях?!
Итак, сегодня мы разберемся, как «поставить колонку». Если пропустили, зачем это нужно – добро пожаловать в Часть 1. Вкратце: допустим, нужно отделить одно белое вещество от другого белого вещества…и от кучи всякого мерзкого.
-сорбент, он же неподвижная фаза
-элюент, он же подвижная фаза, он же какой-либо органический растворитель.
-раствор вашей смеси
-штатив с пробирками
-выдержка и терпение
Сначала поподробнее о лабораторных колонках. Это цилиндрические трубки с сужением на конце, изготовленные из стекла или кварца. Современные для удобства снабжены краном на конце, так что в них можно регулировать поток и останавливать хроматографию в любой момент. Обычные стеклянные колонки не пропускают УФ, так что чтобы следить за ходом хроматографии можно ставить ТСХ с выходящего раствора или, если вам повезло, ориентироваться на цвет идущих пятен. Кварцевые колонки в этом плане удобнее – за продвижением пятна в них можно следить по УФ.
Выбирают колонку в зависимости от масштабов и сложности разделения: на широкой колонке можно поделить больше, на высокой — лучше.
Самым распространенным сорбентом в лабораториях остается силикагель. Он может быть разный по форме, размеру (35-70 мкм, 60-120 мкм, а для промышленных колонок — гораздо меньше) и по распределению частиц по размерам.
Чем более мелкие и однородные по размеру частицы, тем лучше будет разделение. Но за все хорошее приходится платить: мелкий силикагель плотно забивает колонку, так что жидкости будет сложнее проходить. В таком случае для ускорения процесса можно хроматографировать под давлением (т.е. в лаборатории – давить сверху с помощью груши или шприца).
*В качестве сорбента можно использовать не только силикагель, но и оксид алюминия. Михаил Цвет (тот чел, что изобрел препаративную хроматографию) вообще использовал карбонат кальция (попросту мел) для разделения пигментов.
Теперь наконец-то переходим к методике
Шаг 1. Закрепляем колонку на штативе. Если она без крана – затыкаем ее снизу ваткой. Также можно еще насыпать снизу небольшой слой песочка, чтобы покрыть сужение, и силикагель заполнять уже ровным слоем.
Шаг 2. Готовим элюент, который подобрали на первой стадии.
Шаг 3. Готовим суспензию силикагеля в элюенте.
Сколько взять силикагеля? Обычно ориентируются на массу разделяемой смеси и берут в 100 раз больше. То есть, если у нас 200 мг смеси, неплохо бы поделить их на 20 граммах силикагеля как минимум. НО важнейшим критерием для разделения все-таки остается высота колонки. Теми же 20 граммами можно заполнить широкую или узкую колонку, и в зависимости от этого будет различная высота слоя сорбента. При сложном разделении лучше всегда отдавать предпочтение колонке повыше.
Если вы собираетесь проводить хроматографию в кварцевой колонке, и хотите смотреть за передвижением пятен – тут же добавляем УФ-индикатор (1% от массы силикагеля, то есть те же 200 мг, но можно и чуть меньше).
Теперь в сухую смесь остается долить элюент и все это тщательно перемешать. Чтобы максимально приблизиться к состоянию суспензии и выгнать все пузырьки воздуха, смесь обрабатывают на ультразвуке.
Шаг 4. Заполняем колонку. Для этого аккуратно выливаем суспензию силикагеля, следя, чтобы не образовывалось пустот (можно постукивать по колонке палочкой – так силикагель плотнее упакуется). Чтобы вылить весь приготовленный силикагель, остатки можно еще раз залить элюентом и добавить туда же.
Шаг 5. Нанесение вещества. Этот этап очень ответственный, и от него может зависеть весь успех вашего предприятия. Раствор нанести нужно так, чтобы не повредить верхний слой силикагеля. Можно дать ему аккуратно стечь по стенкам (но тогда еще дополнительный этап – смыть остатки со стенок), либо капля за каплей нанести по всему сечению колонки. После нанесения сверху насыпают слой песочка. Это поможет не повредить верхний слой силикагеля при элюировании и одновременно на какое-то время предотвратит пересыхание колонки, если вы проспите забудете подлить элюента.
Шаг 6. Элюирование. Кажется, здесь нет ничего сложного – стой да наливай сверху элюент, снизу собирай свои фракции по пробиркам. Важно не дать колонке пересыхать, иначе сорбент может растрескаться, что ухудшит разделение.
На небольшую колонку может уйти в среднем 200-500 мл элюента, в зависимости от того, какой Rf вашего вещества. Если Rf высокий – вещество выходит с колонки быстро, и большие объемы не понадобятся. Соответственно, при низком Rf элюирование будет долгим и печальным. Но! всегда можно сделать его более радостным, по ходу колонки потихоньку увеличивая полярность элюента. Это называется градиентным элюированием. Его очень удобно применять, если вам надо собрать вещество с низким Rf, но до него выходит еще куча примесей. Тогда первые пятна выгоняют на малополярных элюентах, а по мере их выхода плавно увеличивают полярность.
Следить за продвижением вещества по колонке можно с помощью той же УФ лампы. Вещество будет более темным пятном в сравнении c ярко-зеленым фоном.
Что ж, все собрано, Вы восхитительны!
Теперь с пробирок можно поставить ТСХ, чтобы точно определить в каких нужное вам вещество.
Что может пойти не так:
1. Может быть так, что ваши вещества не растворяются в элюенте. В этом случае можно воспользоваться способом сухого нанесения. Для этого вещество растворяют в подходящем легколетучем растворителе (например, ацетоне). К раствору добавляют немного (пару шпателей) силикагеля, тщательно перемешивают и упаривают. В итоге получается силикагель с равномерно нанесенным на него веществом, который насыпают сверху колонки и дальше элюируют как обычно. Слой силикагеля должен оказаться примерно такой же по уровню, как если бы вы налили раствор вещества.
2. При градиентном элюировании, если вы поспешили и начали увеличивать полярность элюента, не дав выйти первым пятнам, может случиться так, что последние пятна их догонят и перекроются. Поэтому увеличивать полярность желательно только после выхода каждого вещества.
3. Если на колонку загружено мало вещества, то по ходу колонки оно может постепенно исчезнуть из виду и больше не светиться в УФ. Остается по старинке собирать вещество по пробиркам, следя за окончанием по ТСХ или нанося каплю раствора на стекло: если после испарения растворителя остается след – что-то еще идет.
4. Самый тяжелый случай – это когда вещество разлагается на силикагеле. В итоге с колонки выйдет уже не то, что вы туда загрузили. Желательно до начала колонки удостоверится в стабильности вашего вещества на выбранном сорбенте. Это можно проверить с помощью двумерной ТСХ. Делается это так: ставится ТСХ на квадратной пластинке, причем пятно наносится с одного края. Когда элюент доходит до верха, ту же пластинку вынимают и переворачивают так, чтобы снизу оказалась та сторона, по которой прошло вещество. Если после такой операции пятна не увеличатся в количестве и останутся на диагонали, можно смело делить на колонке. В противном случае вам не повезло и придется искать другой способ очистки.
5. Не разделилось! Что ж, этому есть много разных причин: недостаточная высота колонки, неаккуратное нанесение, неплотно заполненная колонка (где-то образуются застойные зоны или наоборот, пустоты или трещины, где жидкость легко проходит), неправильно подобран элюент…
Если разница Rf меньше 0,1-0,2 вообще сложно получить качественное разделение на небольшой колонке. Тогда спасает только полуметровая колонка и очень много терпения.
Собираем нужные фракции и упариваем растворитель.
Описанный метод подпадает под определение жидкостной адсорбционной хроматографии, то есть тут важно, насколько вещество хорошо сорбируется/десорбируется. Кроме этого еще существует ионообменная (когда неподвижная фаза имеет на поверхности заряженные группы, что позволяет разделять ионы по величине заряда), аффинная (основанная на специфическом взаимодействии веществ с определенным лигандом, пришитым на неподвижную фазу, что удобно для очистки биомолекул), гель-проникающая (разделяет вещества по размерам молекул — чем они больше, тем хуже проникают в поры носителя и легче выходят) и другие виды хроматографии, каждый из которых хорош для определенного типа задач.
В следующих сериях рассмотрим еще один метод препаративной хроматографии, который как будто бы создан специально для ЛЛ.)
Лига Химиков
1.2K постов 10.6K подписчика
Правила сообщества
Старайтесь выбирать качественный контент и не ставьте теги моё на копипасты
Посты с просьбой решения домашнего задания переносятся в общую ленту
1. Оскорблять пользователей.
2. Постить материал далеко не по теме и непотребный контент (в остальном грамотно используйте теги)
3. Рекламировать сомнительные сайты и услуги коммерческого характера
Поэтому теоретиком быть лучше)
Хроматография белков на сефадексах. Микроколоночная высокого давления. Тонкослойная бумажная и силикагелевая. Градиентная на ионообменниках. А настройка проточного спектрофотометра. У меня диплом был с темой хроматография пептидов на микроколоночной системе высокого давления в концентрированной трифторуксусной кислоте. Молодость молодость.
А я таким же шприцом со шлангом кактусы поливаю 🙂
Интересно. А можно чуть подробнее о двумерной ТСХ? Есть какие-нибудь примеры неудачных вариантов, когда вещество разлагается? И какую информацию можно извлечь из такой неудавшейся ТСХ?
Сегодня есть ВЭЖХ, какое применение у таких методов? Чтобы студенты научились основам хроматографии?
Оксид серы. Способы получения и химические свойства
А вы знали запах какого вещества человек ощущает когда горит спичка? — А теперь будете знать, это оксид серы (IV). Ещё больше информации про это вещество смотри на видео!)
Выпаривание растворителя из вязкой фосфорорганической кислоты
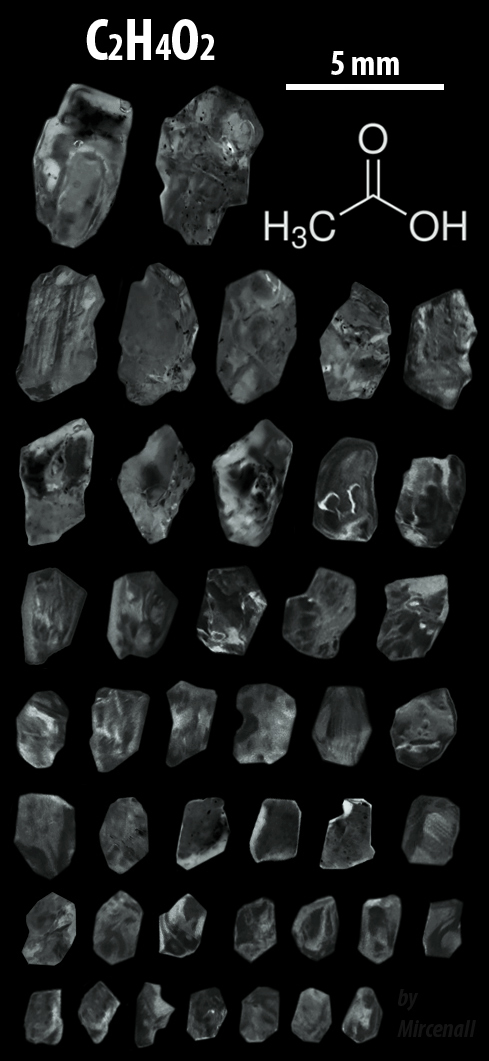
Кристаллы уксусной кислоты
Получены в лаборатории в результате охлаждения концентрированного раствора. Плавятся при температуре выше 16,8 °C
Подобные и прочие посты также на странице ВК:
Другие фотографии кристаллов органических соединений:
Кристаллы продукта реакции фенольного соединения и свободного радикала
Полное название соединения — 3,5-ди-терт-бутил-3-(((2,4-диоксопентан-3-илиден)амино)окси)-4-оксоциклогекса-1,5-диен-1-карбальдегид. Образуется при перехвате свободного радикала (диацетилиминоксила) антиоксидантом (веществом, сходномым с ионолом).
P.S. практических применений у данного вещества нет, его впервые синтезировали всего несколько месяцев назад. Если кратко, то химики-органики, получив диацетилиминоксильный радикал, начали присоединять его ко всему, что можно, дабы продемонстрировать его хорошую реакционную способность (в том числе к рандомному антиоксиданту), в результате открыв вещество, представляющее из себя красивые оранжевые кристаллики, которые и отдали мне сфотографировать)
Подобные и прочие посты также на странице ВК:
Другие фотографии кристаллов органических соединений:
Добро пожаловать в органическую химию!
P.S. На самом деле химическая номенклатура действительно очень важна для унифицирования названий и легкого взаимопонимания между химиками. Но для сложных молекул названия по ИЮПАК становятся достаточно длинными и сложными. Поэтому для наиболее распространенных молекул в химической среде бытуют тривиальные названия, например, анизол/кумол/стирол, которые хоть и ничего не говорят о структуре, но понятны всем. В научном сообществе к ним добавляются самые разнообразные аббревиатуры и условные обозначения типа RaNi (просто никель Ренея, радий не при чем), bipy, dppf, hfacac, DPPH, DEAD, TEA, которые сокращают время написания формул и значительно облегчают жизнь.
Кристаллы 4-бензоилокси-2,2,6,6-тетраметилпиперидин-1-оксила
4-Бензоилокси-2,2,6,6-тетраметилпиперидин-1-оксил (4-BzO-TEMPO) является стабильным свободным радикалом, способным перехватывать другие органические радикалы (служит ловушкой при исследовании механизмов реакции), однако он более селективен, чем сам TEMPO-радикал, дольше живёт и применяется для создания радикальных меток в электронном парамагнитном резонансе
Подобные и прочие посты также на странице ВК:
Другие фотографии кристаллов органических соединений:
Кристаллы 1-этинил-1-циклогексанола
1-Этинил-1-циклогексанол (ECHO) — органическое соединение, получаемое по реакции Фаворского из циклогексанона и ацетилена. Температура плавления вещества всего 30°C и кристаллы в сосуде могут перейти в жидкость даже от тепла рук.
Соединение используется в синтезе органотеллуриевых соединений, ингибирующих активность белка катепсина B, в качестве стабилизатора хлорированных органических соединений, а также реагирует с комплексами гидридов переходных металлов с образованием винильных производных. Вещество огнеопасно, а пары ECHO могут вызывать у человека аллергические реации в виде покраснения глаз.
Подобные и прочие посты также на странице ВК:
Другие фотографии кристаллов органических соединений:
Тонкослойная хроматография чернил в ускоренной съемке
Один из самых простых хроматографических методов анализа, в основе которого лежит способность веществ в смеси по разному сорбироваться в подвижной фазе растворителя из-за чего расстояние, на которое эти компоненты смещаются по слою сорбента за одно и то же время, различается и смесь разделяется.
Тонкослойная хроматография для не-специалистов
Вероятно, все из нас видели (хотя бы на фотографии) тест на беременность. Надеюсь, никому не приходилось встречаться с тест-полосками на наркотики_или проваливать допинг-тесты. И, скорее всего, все читали или смотрели экранизацию “Двенадцати стульев”, где Ипполит Матвеевич Воробьянинов, желая получить «радикальный черный цвет» волос, остался с шевелюрой всех цветов радуги, которую пришлось в итоге сбрить.
Удивительно, но процессы, которые лежат в основе всех примеров – одни и те же. На этих же процессах основан один из очень распространенных методов разделения и определения веществ – так называемая тонкослойная хроматография. Термин тонкослойная» всего лишь означает, что она проводится на слое_толщиной в миллиметр (по сравнению с объемной хроматографией, где толщина вещества-основы может составлять до сантиметра), а вот о том, что же такое «хроматография», стоит рассказать подробнее. В 1903 году русский ученый Михаил Цвет представил на суд ученых новый способ разделения веществ, из которых состоит хлорофилл – зеленый краситель в листьях – и назвал его «цветописью» или хроматографией. Забавное совпадение: человек_по фамилии Цвет работает с красителями и называет новый метод почти в свою честь. Основан этот метод был на отличиях в силах взаимодействия разных молекул с веществом-основой. В качестве последнего в опытах Цвета выступал мел, но сейчас чаще всего используют силикагель (маленькие шарики, которые можно найти в пакетиках с обувью при покупке) или оксид алюминия. Цвет засыпал мелкий порошок мела в вертикальную стеклянную трубку, утрамбовал его, осторожно залил водой (так, чтобы весь мел намок, но не «поплыл») и сверху залил немного раствора хлорофилла. Далее он добавлял воду, а ее избыток вытекал снизу. Постепенно зеленая полоска продвигалась вниз и разделялась на три – светло-зеленую, темно-зеленую и желтоватую. Когда каждая из полосок оказывалась внизу трубки, экспериментатор собирал вытекающую жидкость в отдельный стакан. Оказалось, что хлорофилл состоит из трех разных веществ –их потом назвали хлорофилл А, хлорофилл Б и лютеин. Именно из-за насыщенности цветов метод получит такое название. Почти сразу ученые поняли, что таким образом можно разделять и другие вещества. Сначала опыты ставились на смесях красителей, чтобы было проще определять, когда следует собирать вытекающую жидкость, потом научились работать и с бесцветными веществами, подсвечивая трубку ультрафиолетом, или добавляя реагенты, которые окрашивали соединения. Далее оказалось, что вместо воды можно использовать другие жидкости, и тогда список разделяемых веществ значительно увеличился. С дальнейшим развитием техники научились разделять газы, здесь в качестве жидкости используются азот или благородные газы, а длина трубки может достигать целых 150 м, поэтому ее нужно сворачивают в кольцо. Этот метод стал незаменимым помощником химиков-органиков для очистки получаемого вещества, потому что особенностью органического синтеза является огромное количество разных примесей, и выделение продукта та еще задача; биохимиков, так как один из видов хроматографии – почти единственный способ разделения белков; и химиков-криминалистов для определения состава чернил и доказательства подлинности документа или, например, определения состава наркотических смесей
Вернемся именно к тонкослойной хроматографии – ее можно провести очень быстро (до получаса – обычное время такого анализа, по сравнению с несколькими часами обычной хроматографии), прямо на месте (из оборудования – пластинка с силикагелем, стаканчик с жидкостью и пипетка, а не огромные установки, как для разделения газов) и без химического образования – нужно лишь капнуть образец на край пластинки и аккуратно поставить ее в стакан. За нас все сделают капиллярные силы – растворитель сам будет подниматься вверх. В конце нужно либо опустить пластинку в раствор-проявитель, либо, если вещества с самого начала были цветными, просто посмотреть на нее. Обычно на пластинку ставят две точки – образец (смесь веществ, в которой надо определить наличие чего-либо) и чистое вещество, которое мы ищем. Если на хроматограмме (так называется итоговая картина) образца окажется пятнышко на том же месте, где и на хроматограмме чистого вещества – значит, оно есть в смеси. Все очень просто и доступно даже ребенку. Кстати о детях – если в качестве пластинки использовать прямоугольный или круглый кусочек рыхлой бумаги (в идеале – фильтровальной), то можно разделить пигменты в черном фломастере. Оказывается, черный цвет – это смесь многих цветов, а не единый пигмент. Этот опыт хотя и очень простой, но и очень красивый. При возможности настоятельно рекомендую попробовать! В случае же Кисы Воробьянинова в качестве пластинки выступили его волосы (разные вещества в краске для волос по-разному осели на волосах), и при смывании произошло их разделение. Нерешенным вопросом остались тесты на беременность, допинг и наркотики. Тут тоже все просто – на эти полоски нанесены вещества, которые проявляют окраску только при наличии наркотиков, допинга или гормона ХКЧ (его количество у беременных гораздо больше) в моче. Аналогично, кстати, работают тест-полоски на сифилис, вирус иммунодефицита человека и даже на наличие в образце крови (это очень важно для криминалистов). И, естественно, тест-полоски на коронавирус, если такие появятся в широком доступе, будут основаны именно на продвижении вещества по полоске за счет капиллярных сил.
Вот и получается, что событие, которое было описано в 1928 году, детские эксперименты и современные экспресс-тесты основаны на одном физико-химическом процессе.
Источник